Mit Kunstzucker zu Stahlknochen

Dresdner Biotechnologinnen arbeiten an Selbstheilungs-Therapie für altersschwache Knochen
Dresden, 30. April 2023. An einer Art künstlichen Zuckermolekülen, die altersschwache Knochen womöglich wieder härten und reparieren können, arbeiten derzeit Dresdner Biotechnologinnen und Mediziner gemeinsam mit Berliner Synthese-Experten. Bei Mäusen klappt das auch schon recht gut. Allerdings ist noch abzuklären, ob der Knochenhärtungszucker auch beim Menschen funktioniert. Das geht aus einer Mitteilung der TU Dresden hervor.
Team schaltet mit Designer-Molekülen die Regenerationsbremser aus
Die Grundidee dabei: Bei alten Menschen können sich gebrochene oder abgenutzte Knochen nicht mehr so schnell heilen wie bei Jugendlichen, zudem verlieren sie an Widerstandskraft bis hin zur Osteoporose. Mitschuld daran sind bestimmte Signalmoleküle, die das Knochenwachstum ausbremsen. Um diese Bremser auszutricksen, hat sich in Dresden ein interdisziplinäres Team um Prof. Maria Teresa Pisabarro vom Biotechnologischen Zentrum (Biotec) der TU Dresden, Dr. Vera Hintze vom Max-Bergmann-Zentrum für Biomaterialien und den Knochenexperten Prof. Lorenz Hofbauer von der Medizinischen Fakultät der TU Dresden zusammengetan. „Wir kennen einen bestimmten molekularen Weg, den Wnt-Signalweg, der die Knochenbildung und -reparatur reguliert. Wir konnten ihn auf zwei Bremssignale eingrenzen, die gemeinsam die Knochenregeneration blockieren: Sclerostin und Dickkopf-1“, erklärte Prof. Lorenz Hofbauer. „Die große Herausforderung für die Entwicklung von Medikamenten, zur Verbesserung der Knochenheilung, besteht darin, diese beiden Blockade-Proteine gleichzeitig und effizient auszuschalten.“
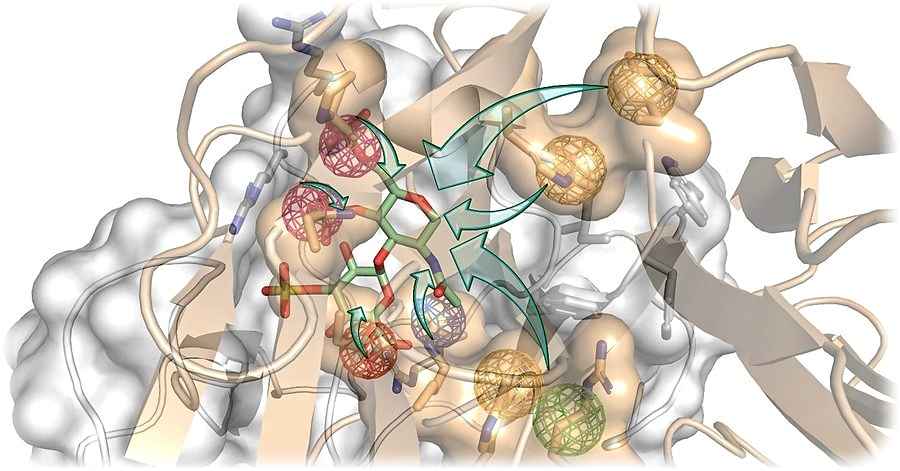
Langkettiges Zuckermolekül am Rechner entworfen
Daher entwarfen die Dresdner am Computer künstliche Biomoleküle, die langkettigen Zuckern wie Hyaluronsäure oder Heparin ähneln und die die Brems-Moleküle ausschalten können. „Mit Hilfe von Molecular Modelling haben wir neue Strukturen entworfen, welche die relevanten Rezeptorinteraktionen mit den beiden Proteinen nachahmen“, erläuterte Professorin Pisabarro. „Wir wollten, dass diese Bindung stärker ist, als ihre natürlichen Wechselwirkungen. Auf diese Weise würden unsere neuen Moleküle die Proteine sowohl einfangen und effektiv ausschalten und dadurch die Knochenregeneration fördern.“
Regenerationsquote bei Mäusen um 50% verbessert
Experten der FU Berlin haben diesen Designer-Zucker dann synthetisiert. Hofbauers Knochenlabor-Team hat diese Moleküle schließlich Mäusen mit Knochendefekten eingesetzt. Ergebnis: Die Regeneration der Mäuseknochen verbesserte sich um 50 Prozent. Dies weise auf „ein enormes regeneratives Potenzial“ hin, schätzen die TU-Experten ein.
Team will nun Übertragbarkeit auf den Menschen ausloten
Die Forschungsgruppe will nun Geld für eine präklinischen Studie beantragen, „um diese Moleküle als innovative Therapie für eine Studie an Menschen weiterzuentwickeln“, kündigte Professor Hofbauer an. Denn die neu entwickelten Moleküle könnten zur Entwicklung neuer, wirksamerer Therapien für Knochenbrüche und andere Knochenerkrankungen führen.
Autor: hw
Quelle: TUD
Wissenschaftliche Publikation:
Gloria Ruiz-Gómez, Juliane Salbach-Hirsch, Jan-Niklas Dürig, Linda Köhler, Kanagasabai Balamurugan, Sandra Rother, Sophie-Luise Heidig, Stephanie Moeller, Matthias Schnabelrauch, Giulia Furesi, Sophie Pählig, Pedro M. Guillem-Gloria, Christine Hofbauer, Vera Hintze, M. Teresa Pisabarro, Jörg Rademann, Lorenz C. Hofbauer: „Rational engineering of glycosaminoglycan-based Dickkopf-1 scavengers to improve bone regeneration“, in: Biomaterials (April 2023) Link: https://doi.org/10.1016/j.biomaterials.2023.122105

Ihre Unterstützung für Oiger.de!
Ohne hinreichende Finanzierung ist unabhängiger Journalismus nach professionellen Maßstäben nicht dauerhaft möglich. Bitte unterstützen Sie daher unsere Arbeit! Wenn Sie helfen wollen, Oiger.de aufrecht zu erhalten, senden Sie Ihren Beitrag mit dem Betreff „freiwilliges Honorar“ via Paypal an:
Vielen Dank!


